В ЄС рекомендували ремдесивір як препарат для лікування COVID-19
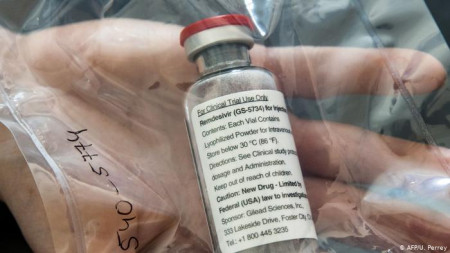
Європейське агентство з лікарських засобів (EMA) у четвер, 25 червня, рекомендувало схвалити препарат ремдесивір як ліки проти COVID-19. Це перший препарат, що отримав дозвіл на використання від ЕМА, зазначається на сайті агентства, пише DW.
«Дані про ремдесивір були оцінені у винятково короткі строки за допомогою особливої процедури, що використовується ЕМА під час надзвичайних ситуацій в галузі охорони здоров’я для оцінки даних в міру того, як вони надходять», – йдеться в заяві.
За результатами оцінки препарату надана рекомендація, заснована в основному на даних дослідження NIAID-ACTT-11, що спонсорується Націнститутом алергії та інфекційних захворювань США (NIAID), а також на даних інших досліджень ремдесивіра.
У дослідженні NIAID-ACTT-1 оцінювалася ефективність 10-денного курсу лікування ремдесивіром у понад 1000 пацієнтів, госпіталізованих з COVID-19. Ремдесивір порівнювали з плацебо (фіктивне лікування), і основним показником ефективності був час одужання пацієнтів.
У цілому дослідження показало, що пацієнти, які отримували ремдесивір, одужували приблизно через 11 днів, у порівнянні з 15 днями для пацієнтів, які отримували плацебо. Цей ефект не спостерігався у пацієнтів з легким та середнім ступенем тяжкості захворювання: час до одужання становив 5 днів як для групи ремдесивіру, так і для групи плацебо. Для пацієнтів з важким перебігом хвороби, які становили приблизно 90 відсотків досліджуваної групи, час до одужання становив 12 днів у групі ремдесивіру та 18 днів у групі плацебо.
Згідно з рекомендацією, препарат має бути схвалений для лікування COVID-19 у дорослих і підлітків віком від 12 років, які мають пневмонію і які потребують додаткового кисню.
Ця рекомендація потребує схвалення у Єврокомісії, яка має ухвалити рішення наступного тижня.
Як повідомлялося, управління з санітарного нагляду за якістю продовольства та медикаментів міністерства охорони здоров’я США (FDA)видало екстрений дозвіл на використання у виняткових випадках препарату ремдесивір у лікарнях пацієнтами з атиповою пневмонією COVID-19 ще на початку травня.
Ремдесивір був розроблений американською біотехнологічною компанією Gilead Sciences для боротьби з лихоманкою Ебола, а пізніше показав ефективність у боротьбі зі збудниками коронавірусів SARS і MERS.
Підписуйтесь на наш Telegram-канал, аби першими дізнаватись найактуальніші новини Волині, України та світу
«Дані про ремдесивір були оцінені у винятково короткі строки за допомогою особливої процедури, що використовується ЕМА під час надзвичайних ситуацій в галузі охорони здоров’я для оцінки даних в міру того, як вони надходять», – йдеться в заяві.
За результатами оцінки препарату надана рекомендація, заснована в основному на даних дослідження NIAID-ACTT-11, що спонсорується Націнститутом алергії та інфекційних захворювань США (NIAID), а також на даних інших досліджень ремдесивіра.
У дослідженні NIAID-ACTT-1 оцінювалася ефективність 10-денного курсу лікування ремдесивіром у понад 1000 пацієнтів, госпіталізованих з COVID-19. Ремдесивір порівнювали з плацебо (фіктивне лікування), і основним показником ефективності був час одужання пацієнтів.
У цілому дослідження показало, що пацієнти, які отримували ремдесивір, одужували приблизно через 11 днів, у порівнянні з 15 днями для пацієнтів, які отримували плацебо. Цей ефект не спостерігався у пацієнтів з легким та середнім ступенем тяжкості захворювання: час до одужання становив 5 днів як для групи ремдесивіру, так і для групи плацебо. Для пацієнтів з важким перебігом хвороби, які становили приблизно 90 відсотків досліджуваної групи, час до одужання становив 12 днів у групі ремдесивіру та 18 днів у групі плацебо.
Згідно з рекомендацією, препарат має бути схвалений для лікування COVID-19 у дорослих і підлітків віком від 12 років, які мають пневмонію і які потребують додаткового кисню.
Ця рекомендація потребує схвалення у Єврокомісії, яка має ухвалити рішення наступного тижня.
Як повідомлялося, управління з санітарного нагляду за якістю продовольства та медикаментів міністерства охорони здоров’я США (FDA)видало екстрений дозвіл на використання у виняткових випадках препарату ремдесивір у лікарнях пацієнтами з атиповою пневмонією COVID-19 ще на початку травня.
Ремдесивір був розроблений американською біотехнологічною компанією Gilead Sciences для боротьби з лихоманкою Ебола, а пізніше показав ефективність у боротьбі зі збудниками коронавірусів SARS і MERS.
Знайшли помилку? Виділіть текст і натисніть
Підписуйтесь на наш Telegram-канал, аби першими дізнаватись найактуальніші новини Волині, України та світу

Коментарів: 0
Відправив «Новою поштою» автомат і гвинтівку до Луцька: сержанта судили за збут зброї
Сьогодні 16:12
Сьогодні 16:12
В Україні вже оголошено понад 180 підозр у схемах ухилення через ТЦК та лікарські комісії
Сьогодні 15:43
Сьогодні 15:43
Римма Зюбіна, зіркове журі та фіналісти: 13-й Чілдрен Кінофест оголошує ключові імена
Сьогодні 15:14
Сьогодні 15:14
Волинянка заявила, що її чоловіка та 14-річного сина побили люди в балаклавах. Що кажуть у Волинському ТЦК
Сьогодні 14:16
Сьогодні 14:16
Росія через соцмережі та ШІ розганяє фейк про нашестя мігрантів в Україні, а українці потурають брехні. Дослідження
Сьогодні 13:47
Сьогодні 13:47
У Володимирі через несправність гальм спалахнуло авто
Сьогодні 13:18
Сьогодні 13:18
Безпека, інклюзія, комфорт: у Волинській обласній дитячій лікарні триває реконструкція
Сьогодні 12:30
Сьогодні 12:30
Ворожий дрон атакував на Рівненщині приватне підприємство
Сьогодні 12:01
Сьогодні 12:01
На Трійцю до Луцька приїде глава ПЦУ Епіфаній
Сьогодні 11:32
Сьогодні 11:32




























Додати коментар:
УВАГА! Користувач www.volynnews.com має розуміти, що коментування на сайті створені аж ніяк не для політичного піару чи антипіару, зведення особистих рахунків, комерційної реклами, образ, безпідставних звинувачень та інших некоректних і негідних речей. Утім коментарі – це не редакційні матеріали, не мають попередньої модерації, суб’єктивні повідомлення і можуть містити недостовірну інформацію.